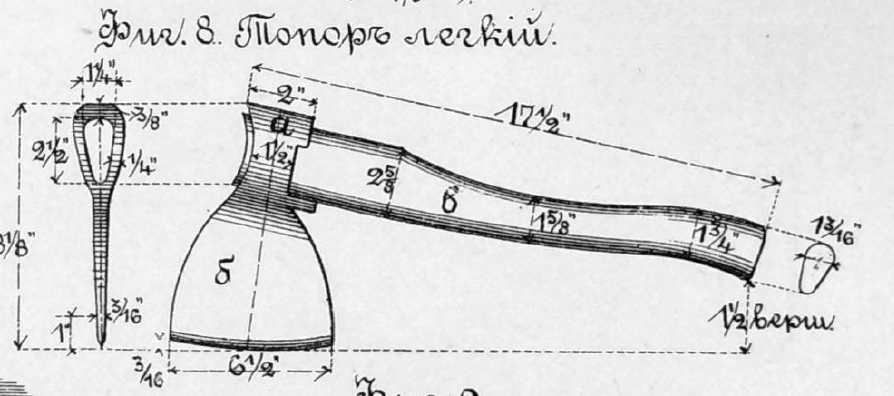
Боевые топоры, история развития, разновидности, строение и конструктивные особенности.
Боевые топоры это разновидность ударного оружия рубящего действия. Топоры состоят из ударной части — железки и рукояти — топорища. Появились боевые топоры в раннем каменном веке, изначально в качестве инструмента. Впоследствии небольшие каменные, а затем и металлические топорики стали использоваться как оружие.
Боевые топоры, история развития, разновидности, строение и конструктивные особенности.
В античную эпоху боевые топоры не получили широкого распространения. Зато в период раннего Средневековья боевой топор стал крайне популярным оружиемближнего боя. Благодаря своим выдающимся рубящим свойствам топор мог эффективно поражать основной тип защиты того времени — кольчугу. С появлением сплошного латного доспеха боевые топоры постепенно ушли на второй план, а впоследствии превратились в парадное оружие.
Схема строения топора.
Разновидности боевых топоров.

Все топоры можно условно разделить на три группы. К первой группе относятся рабочие топоры — инструменты для рубкидров и прочих хозяйственных нужд. В боевых целях рабочие топоры использовались достаточно редко, в силу их большой массы и размеров.
Ко второй группе относятся боевые топоры, предназначенные непосредственно для боя. В хозяйственных целях такое оружие также использовали лишь в исключительных случаях. Наконец, третью группу составляют топоры универсального типа, при необходимости используемые и в качестве хозяйственно-бытового инструмента, и как оружие.
Боевые топоры можно, в свою очередь, разделить на две основные группы. Первая группа — небольшие топорики, предназначенные для боя одной рукой. Это, как правило, топорики всадников, хотя среди пехотинцев такое оружие также было популярным.
Вторая группа — большие боевые топоры, с топорищем длиной более 1 метра, предназначенные для боя двумя руками. Такие топоры предназначались исключительно для пешего строя.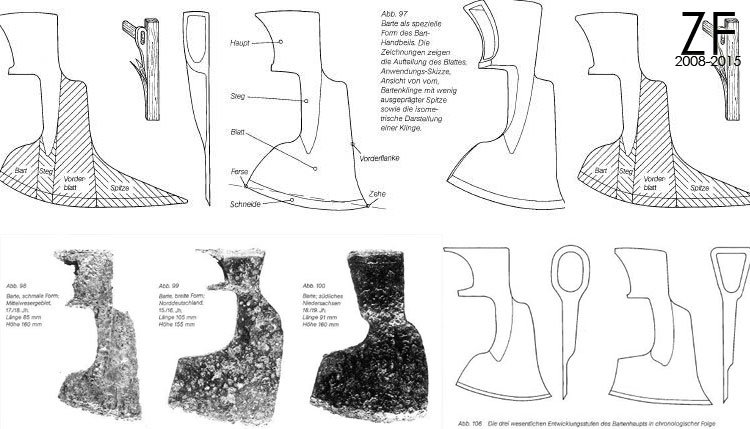 Как правило, ими вооружались наиболее опытные и сильные воины. Отдельного упоминания заслуживают боевые топоры на рукояти длиннее 1,5 метра, которые можно отнести уже скорее к древковому оружию.
Как правило, ими вооружались наиболее опытные и сильные воины. Отдельного упоминания заслуживают боевые топоры на рукояти длиннее 1,5 метра, которые можно отнести уже скорее к древковому оружию.
Конструктивные особенности боевых топоров.
Боевой топор как оружие имеет ряд конструктивных особенностей, накладывающих определенный отпечаток на технику боя. Главная особенность боевого топора — центр тяжести, смещенный к ударной части, из-за чего удар топора получается более сильным, чем удар меча, но более медленным. Кроме того, удартопором требует достаточно широкого замаха, то есть наличия свободного пространства, что в условиях пехотного строя не всегда приемлемо.
Принято также считать, что производство топора проще, а значит, дешевле изготовления меча. Как следствие, считается, что боевой топор был оружием простых бойцов, в то время как знатные воины предпочитали меч. Однако на практике предпочтение тому или иному типу оружия отдавалось не только по материальным причинам, но и с учетом военнойтактики и индивидуальных пристрастий воина.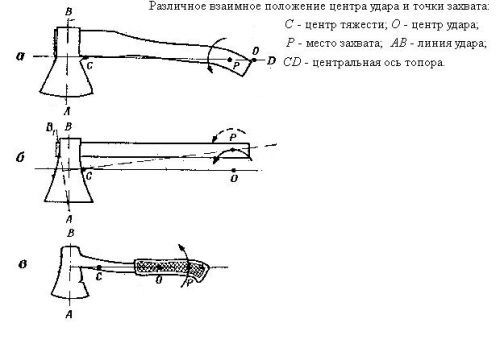
По материалам книги Малая энциклопедия холодного оружия.
Павел Югринов.
Как насадить топор на топорище
От того, как насадить топор на топорище, зависит многое. Качество инструмента, ответственный подход к его подготовке и обслуживанию определяют, удобной ли будет работа и насколько хорошим будет результат ее выполнения. Это особенно актуально, если речь идет о ручном инструменте, использование которого предполагает значительные и непрерывные динамические нагрузки.
Фото 1. Топор может быть предназначен для разной работы, конечный результат которой зависит от качества его насадки на топорище.
Существуют десятки видов топоров, каждый имеет свои конструкционные особенности и предназначение. Плотницкий топор значительно отличается от туристического, топор дровосека совсем не такой, как боевой топор. Но общее одно – это принципиальное строение. Топорище и собственно топор, его металлическая часть, главные составляющие части этого универсального инструмента. И то, как они между собой сочетаются, во многом определяет качество топора.
И то, как они между собой сочетаются, во многом определяет качество топора.
Способы крепления топорищ в топорах
Современные технологии позволяют многое даже для такого инструмента, как топор. Есть несколько способов крепления топорища в топоре:
- сварка;
- изготовление цельнометаллического инструмента;
- склеивание с применением эпоксидного клея, отвердение которого происходит в специальных камерах;
- насаживание и после него расклинивание.
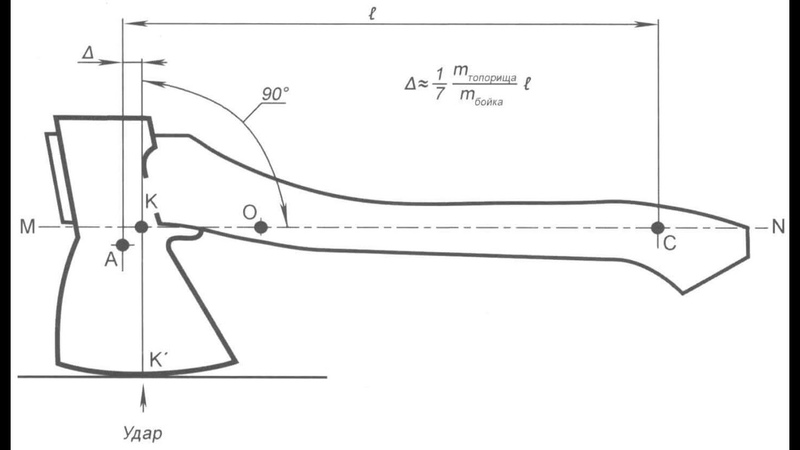
Рисунок 1. Различное взаимное положение центра удара и точки захвата у топора.
Качественно сваренный или цельнометаллический топор совершенно надежен с точки зрения целостности. Поломать его довольно проблематично даже при желании. Проблема только в том, что таким инструментом очень тяжело работать. Он жесткий, отдача очень сильная, руки это чувствуют с первого удара. Профессионалы считают, что такой топор сушит руки.
Склеенный в заводских условиях топор имеет хорошую амортизацию, держится крайне надежно.
В обычных условиях принято насаживать топор на топорище. Следующий этап – расклинивание, оно окончательно определяет надежность соединения. Такой подход, естественно, отличается ярко выраженными недостатками. Он требует хорошей квалификации, достаточно много времени для работы, не всегда дает требуемый результат. Но, с другой стороны, это наиболее доступный способ соединения, для него не нужны ни особые условия, ни особо сложные инструменты. А если конструкция расшатается, все операции можно повторить.
Вопреки кажущейся простоте, правильно насадить топор на топорище не так просто, есть достаточно много нюансов и способов выполнения такой работы.
Вернуться к оглавлению
Подготовительный этап
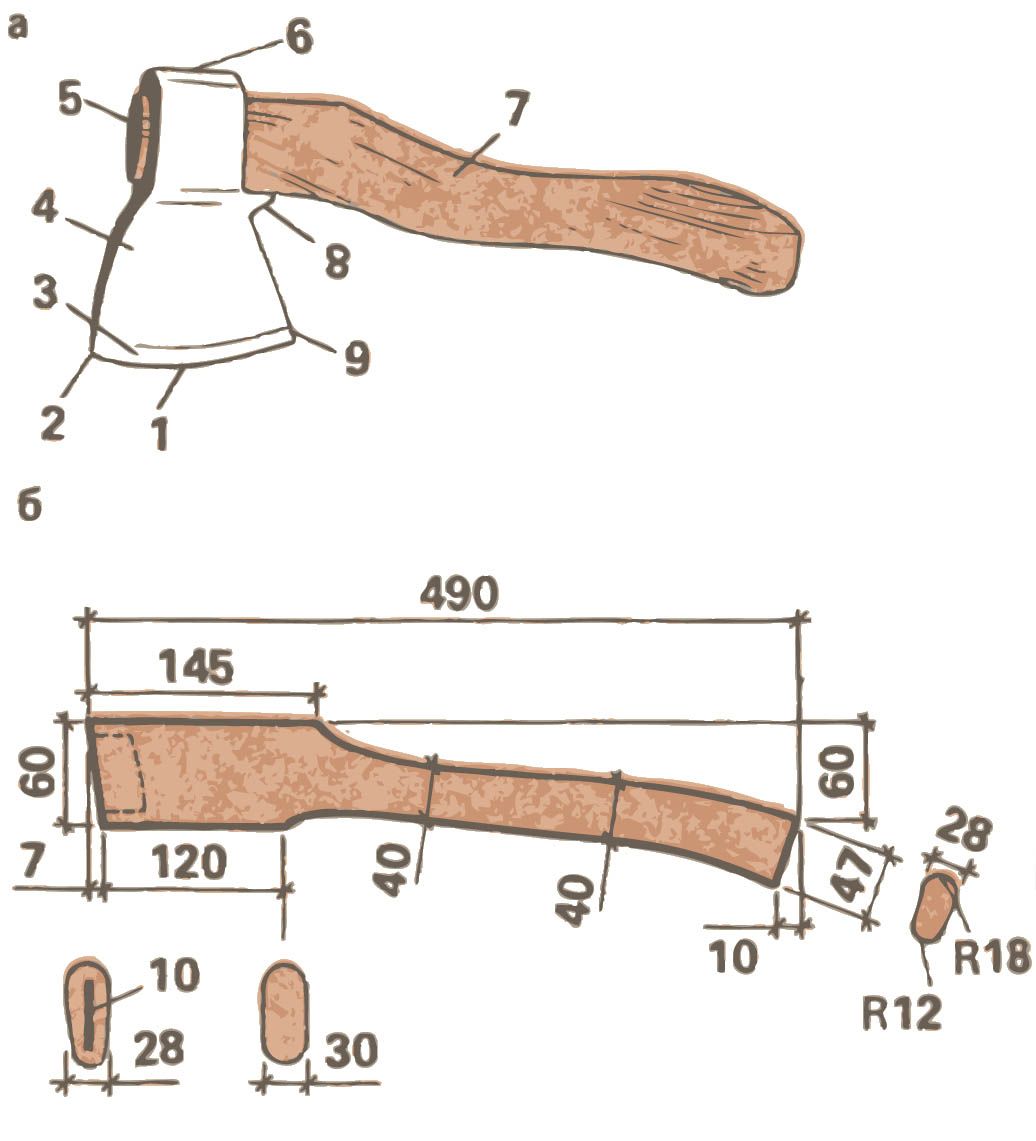
Чертеж изготовления топорища.
Каждая работа, даже самая простая, состоит из нескольких этапов. Сборка топора не исключение. Для того чтобы получить готовый к работе инструмент, необходимо:
- подобрать топорище;
- правильно подогнать его под проушину;
- сделать необходимое количество пропилов;
- подготовить клинья, деревянные или металлические;
- насадить топор;
- расклинить топорище одним из способов.
Четыре первые стадии можно считать подготовительным этапом.
Итак, перед тем как насадить топор на топорище, последнее надо подобрать и приобрести. Что касается материала, то профессиональные плотники и дровосеки рекомендуют хорошо просушенную березу. Этот материал достаточно распространенный, а также обладает свойствами, создающими удобство при работе с инструментом. Более твердые породы дерева хорошо подойдут для декоративных вариантов, но не для рабочих. Наиболее удобная форма топорища, дающая наименьшую отдачу на руки, давно определена.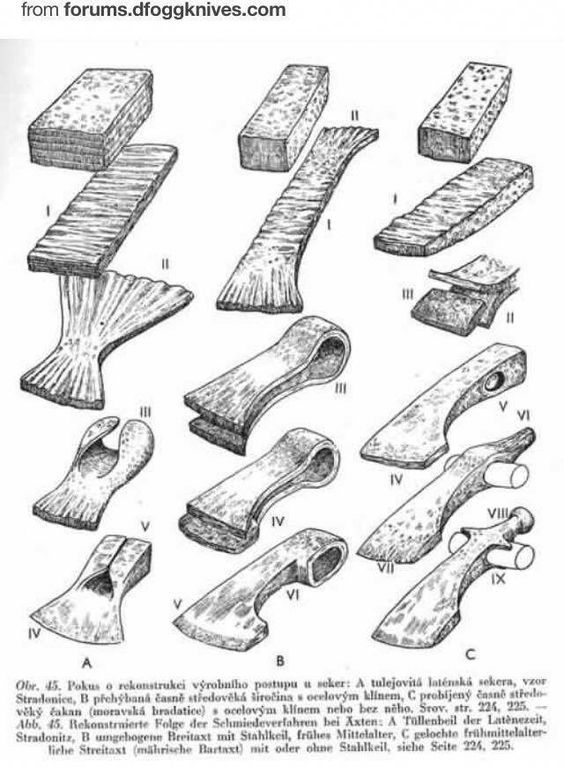
Виды лезвий для топора.
Подогнать топорище под проушину – значить обтесать его до необходимой формы. Для этого пригодится какой-либо деревообрабатывающий инструмент, например, другой топор, острый нож и тому подобное. И тут есть один момент, который необходимо учитывать обязательно.
Ось лезвия топора и продольная ось топорища должны находиться в одной плоскости. Проще говоря, лезвие нужно выровнять относительно топорища.
Несколько слов о проушине. Она может быть как прямой формы, так и в определенной части топора конической. Коническая форма проушины считается более подходящей для хорошего крепления. Перед обтесыванием топорища нужно внимательно подгонять форму.
Наступил черед пропилов на верхнем торце топорища. Их количество определяется выбранным способом расклинивания, которых достаточно много.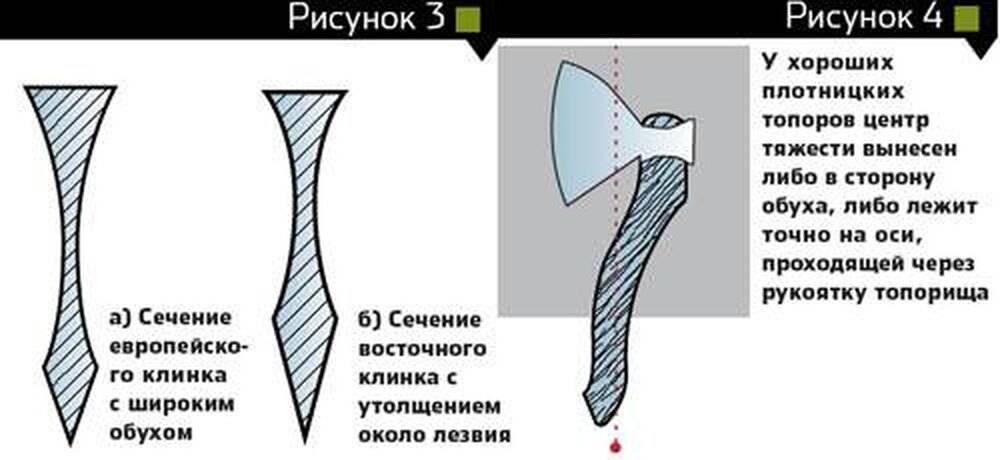 Это может быть всего один продольный паз, может быть два-три боковых, один продольный.
Это может быть всего один продольный паз, может быть два-три боковых, один продольный.
Многие профессиональным считают один продольный и четыре боковых. Это можно увидеть на фото 1, но это далеко не все варианты. Можно выбрать и некоторое смещение пропилов и разделенный на несколько частей продольный пропил. Многие решают этот вопрос исходя из собственных представлений о механических свойствах такого рода соединений.
Рисунок 2. Схема насадки топора на топорище.
Особое внимание необходимо обратить на глубину и ширину пропилов. Глубина должна быть такой, чтобы получившийся паз полностью прятался в проушине. В противном случае топорище может быть расколото при расклинивании или при работе. Ширина пропила должна соотноситься с толщиной клиньев. Клин не должен входить в пропил слишком легко, тогда в нем не будет никакого смысла, но и не должен входить слишком туго, тогда его не удастся вбить внутрь.
Деревянные или металлические клинья (рис. 2) можно купить или изготовить самостоятельно. Тот и другой способ подойдут одинаково хорошо. Стоят они недорого, но если купить негде, можно попросту вырезать их из хорошо просушенной березы. Форма и размеры должны соответствовать параметрам пропилов. Металлический клин можно изготовить из достаточно твердой жести, например, из ненужной совковой лопаты. (рис. 2)
Тот и другой способ подойдут одинаково хорошо. Стоят они недорого, но если купить негде, можно попросту вырезать их из хорошо просушенной березы. Форма и размеры должны соответствовать параметрам пропилов. Металлический клин можно изготовить из достаточно твердой жести, например, из ненужной совковой лопаты. (рис. 2)
Если подготовительный этап пройден правильно, дальше никаких особых проблем возникнуть не должно.
Вернуться к оглавлению
Насаживание и расклинивание
Пришел черед двух последних этапов подготовки топора к работе. Сначала насаживание – топор должен плотно сидеть на топорище, а также ровно, в соответствии с тем, что написано выше. Верхний срез топорища может находиться вровень с верхним срезом топора, а может немного выступать. Главное, чтобы пропил был достаточно глубоким, но не превышал допустимый предел.
После насаживания берется сначала продольный клин, вставляется в пропил и легкими ударами молотка забивается вовнутрь. Слишком сильные удары не нужны, ими можно только расплющить древесину, сделав соединение не столь устойчивым, как хотелось бы. Если клин будет немного выступать, лишнее можно потом срезать ножовкой.
Если клин будет немного выступать, лишнее можно потом срезать ножовкой.
Схема заточки топора своими руками.
Те же манипуляции проделываются с другими клиньями. Можно их посадить на клей, например, эпоксидный. Но это не обязательно, хорошо расклиненное топорище и так будет надежно держаться в проушине.
Металлический клин вбивается сбоку от продольного так, чтобы выступающей части хватило для вбивания с другой стороны деревянного клина. (рис. 2) Металл добавит конструкции надежности и устойчивости.
Верхнюю часть топорища остается зачистить наждачной бумагой и, при желании, залить клеем или покрасить. Тогда будет меньше шансов загнать в руку скалку.
Под конец необходимо провести испытание готового топора. Если ничего не шатается, при ударах все держится надежно, амортизация на должном уровне – инструмент готов к работе.
Обычно тем, кто работает топором постоянно, приходится довольно часто повторять описанную выше процедуру. Для тех, кто берет в руки этот деревообрабатывающий инструмент время от времени, качественного соединения хватит надолго, особенно если не оставлять топор под дождем или не держать его во влажном помещении.
Вернуться к оглавлению
Заключение по теме
Рассмотрена фактически сборка топора, приведение его в рабочее состояние. Чем аккуратнее выполнена эта работа, тем лучше. И лучше выполнять ее самостоятельно, тогда будет точно известно, насколько крепко все держится.
Соблюдение правил техники безопасности – важное условие для работы с любыми колющими и режущими инструментами.
Осторожность и отсутствие спешки сберегут от травм, порезов и других неприятных последствий.
форм молекул
В двухатомной молекуле (X 2 или XY) имеется только одна связь, и полярность этой связи определяет полярность молекулы: если связь полярна, молекула полярна, а если связь неполярна, молекула неполярна.
В молекулах с более чем одной связью обе формы
и полярность связи определяют, является ли молекула полярной .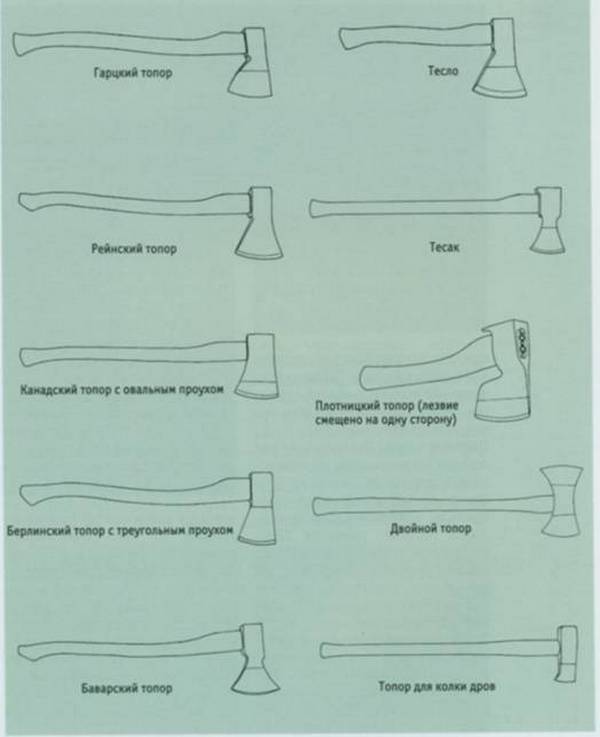 А
молекула должна содержат полярные связи, чтобы молекула была полярной,
но если полярные связи выровнены точно напротив друг друга, или если
они достаточно симметричны, полярность связи уравновешивается, что делает
молекула неполярная. (Полярность является векторной величиной, поэтому оба
величина и направление должны быть приняты во внимание.)
А
молекула должна содержат полярные связи, чтобы молекула была полярной,
но если полярные связи выровнены точно напротив друг друга, или если
они достаточно симметричны, полярность связи уравновешивается, что делает
молекула неполярная. (Полярность является векторной величиной, поэтому оба
величина и направление должны быть приняты во внимание.)
Например, рассмотрим точечную структуру Льюиса для углекислый газ. Это линейная молекула, содержащая два полярных двойные связи углерод-кислород. Однако, поскольку полярные связи направлены ровно на 180 градусов друг от друга, полярности связей компенсируются, и молекула неполярна. (В качестве аналогии вы можете представить себе, что это как игра в перетягивание каната между двумя командами, которые тянут веревку одинаково тяжело.)
Молекула воды также содержит полярные связи, но
поскольку это изогнутая молекула, связи расположены под углом друг к другу
около 105. Они , а не сокращают, потому что они не указывают
точно друг к другу, и есть общий диполь, идущий от
водородный конец молекулы ближе к кислородному концу молекулы;
поэтому вода является полярной молекулой:
Они , а не сокращают, потому что они не указывают
точно друг к другу, и есть общий диполь, идущий от
водородный конец молекулы ближе к кислородному концу молекулы;
поэтому вода является полярной молекулой:
Молекулы, в которых все атомы, окружающие центральные атомы одинаковы, имеют тенденцию быть неполярными, если нет неподеленных пар на центральном атоме. Если некоторые из атомов, окружающих центральный атом различны, однако молекула может быть полярной. например, углерод тетрахлорид, CCl 4 , неполярный, но хлороформ, CHCl 3 , и метилхлорид, CH 3 Cl полярны:
Полярность молекулы сильно влияет на ее
физические свойства. Молекулы, которые более полярны, имеют более сильную
межмолекулярные силы между ними и имеют, как правило, более высокую температуру кипения
точки (а также другие различные физические свойства).
В таблице ниже показано, соответствуют ли примеры в предыдущие разделы являются полярными или неполярными. Для видов, имеющих общий заряд, вместо него используется термин «взимаемый», поскольку термины полярные и неполярные на самом деле не относятся к заряженным частицам; взимается виды по определению существенно полярны. Одиночные пары на некоторых внешних атомы опущены для ясности.
| Формула | Льюис Структура | 3D-структура Форма Полярность | Пояснение |
1. | Ч 4 | четырехгранный неполярный | Связь CH
неполярный, так как C и H отличаются всего на 0,35
единицы электроотрицательности. | |
2. | НХ 3 | треугольный пирамидальный полярный | С тех пор молекула не плоская, связи NH не направлены непосредственно друг на друга, и их полярности не отменяют вне. Кроме того, имеется небольшой диполь в направлении одинокой пары. | |
3. | Н 2 О | изогнутый полярный | С тех пор молекула изогнута, связи ОН не направлены прямо на друг друга, и их полярности не уравновешиваются. | |
4. | Н 3 О + | треугольный пирамидальный заряжен | С тех пор
виды заряжены, термины полярные и неполярные
не имеющий отношения. | |
5. | HCN | линейный полярный | Линейные молекулы обычно неполярны, но в этом случае не все атомы связанные с центральным атомом, одинаковы. Облигация CN полярна и не компенсируется неполярной связью CH. | |
6. | СО 2 | линейный неполярный | Полярный C=O связи ориентированы на 180 градусов друг от друга. Полярность этих связей уравновешивается, делая молекулу неполярной. | |
7. | ККл 4 | четырехгранный неполярный | Полярный CCl
связи ориентированы на 109,5 друг от друга. | |
8. | COCl 2 | треугольная планарная полярный | Тригональная планарная молекулы обычно неполярны, но в этом случае не все атомы, связанные с центральным атомом, одинаковы. полярность связи не компенсируется полностью, и молекула полярна. (Если было три O или три Cls прикрепленный к центральному C, он был бы неполярным.) | |
9. | О 3 | изогнутый полярный | Изогнутые молекулы
всегда полярны. Хотя кислород-кислородные связи
неполярный, неподеленная пара на центральном O вносит некоторый вклад
полярность молекулы. | |
10. | СО 3 2- | треугольная планарная заряжен | С тех пор виды заряжены, термины полярные и неполярные не имеющий отношения. | |
11. | С 2 Н 6 | четырехгранный неполярный | Оба атома углерода четырехгранные; поскольку связи CH и связь CC неполярный, молекула неполярная. | |
12. | С 2 Н 4 | треугольная планарная неполярный | Оба атома углерода
тригонально-плоские; поскольку связи CH и связь CC
неполярны, молекула неполярна. | |
13. | CH 3 CH 2 ОН | C: тетраэдрический О: изогнутый полярный | CC и CH связи не влияют на полярность молекулы, но связи CO и OH полярны, так как форма вокруг атом О изогнут, молекула должна быть полярной. | |
14. | БФ 3 | треугольная планарная неполярный | С тех пор молекула плоская, все три полярные связи BF находятся в той же плоскости, ориентированной на 120° друг от друга, что делает молекула неполярная. | |
15. | № | линейный полярный | Так как есть
только одна связь в этой молекуле, и связь полярная, т. | |
16. | ПКл 5 | треугольный бипирамидальный неполярный | Связи PCl в экваториальные положения этой молекулы ориентированы на 120 друг от друга, и полярность их связей уравновешивается. Связи PCl в аксиальных положениях отстоят на 180° от друг друга, и полярность их связей также уравновешивается. | |
17. | СФ 6 | восьмигранный неполярный | Облигации SF в все эти молекулы находятся на расстоянии 90° друг от друга, и их полярность связи уравновешивается. | |
18. | СФ 4 | качели полярный | Облигации SF в
осевые положения отстоят друг от друга на 90°, а их полярность связи
отменяет. | |
19. | XEF 4 | квадратный плоский неполярный | Облигации XeF все ориентированы на 90° друг от друга, и их связь полярности уравновешиваются. Одинокие пары находятся на расстоянии 180° от друг друга, и их небольшие полярности также уравновешиваются. | |
20. | H 2 SO 4 | S: четырехгранный О: изогнутый полярный | Эта молекула полярны из-за изогнутых связей HOS, которые присутствуют в это. |
Единичных ячеек
Единичных ячеек
| Простейший повторитель в кристалле | А Трехмерный график |
| NaCl и ЗНС | Измерение Расстояние между частицами |
| Определение единицы измерения Ячейка кристалла | Расчет металлик или Ионные радиусы |
Элементарные ячейки: Простейшая повторяющаяся единица в кристалле
Структуру твердых тел можно описать так, как если бы они были
объемные аналоги куска обоев. Обои имеют
регулярный повторяющийся дизайн, который простирается от одного края до другого
другой. Кристаллы имеют похожий повторяющийся рисунок, но в данном случае
дизайн простирается в трех измерениях от одного края твердого тела
к другому.
Обои имеют
регулярный повторяющийся дизайн, который простирается от одного края до другого
другой. Кристаллы имеют похожий повторяющийся рисунок, но в данном случае
дизайн простирается в трех измерениях от одного края твердого тела
к другому.
Мы можем однозначно описать кусок обоев по указание размера, формы и содержания простейших повторяющаяся единица в конструкции. Мы можем описать трехмерное кристалла, указав размер, форму и содержимое простейшая повторяющаяся единица и то, как эти повторяющиеся единицы складываются для формирования кристалла.
Простейшая повторяющаяся единица в кристалле называется единицей . ячейка . Каждая элементарная ячейка определяется в терминах точек решетки точки пространства, вокруг которых частицы могут свободно колебаться. кристалл.
Структуры элементарной ячейки для различных солей показано ниже.
В 1850 году Огюст Браве показал, что кристаллы можно разделить
на 14 элементарных ячеек, отвечающих следующим критериям.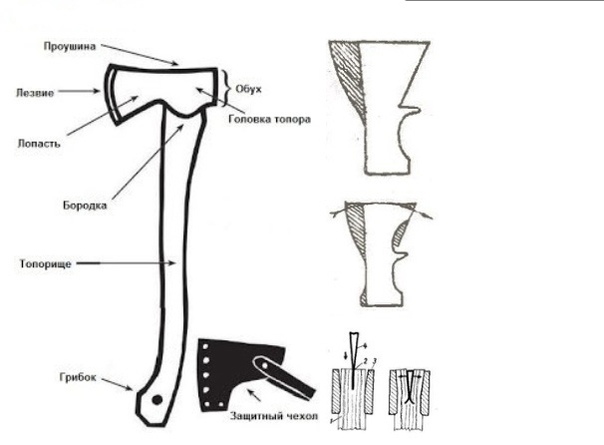
- Элементарная ячейка — простейшая повторяющаяся единица в кристалл.
- Противоположные грани элементарной ячейки параллельны.
- Ребро элементарной ячейки соединяет эквивалентные точки.
14 элементарных ячеек Браве показаны на рисунке ниже.
Эти элементарные ячейки делятся на семь категорий, различающихся три длины ребра элементарной ячейки ( a , b и c ) и три внутренних угла (a, � и g), как показано в таблице ниже.
Семь категорий элементарных ячеек Браве
| Категория | Длина кромки | Внутренние уголки | ||
| Кубический | ( а = б = в ) | ( a = �/i> = g = 90 o ) | ||
| Тетрагональный | ( а = б в ) | ( a = �/i> = g = 90 o ) | ||
| Моноклиника | ( а б в ) | ( a = х/i> = 90 или г) | ||
| Ромбическая | ( а б в ) | ( a = �/i> = g = 90 o ) | ||
| Ромбоэдрический | ( а = б = в ) | ( а = �/i> = г 90 или ) | ||
| Шестигранник | ( а = б в ) | ( a = �/i> = 90 o , g = 120 o ) | ||
| Триклиника | ( а б в ) | ( а �/i> г 90 или ) |
Мы сосредоточимся на кубической категории, которая включает в себя три
типы элементарных ячеекпростые
показан куб, объемно-центрированный куб и гранецентрированный куб
на рисунке ниже.
Эти элементарные ячейки важны по двум причинам. Первый количество металлов, ионных твердых тел и интерметаллических соединений кристаллизуются в элементарных кубических ячейках. Во-вторых, относительно легко выполнять вычисления с этими элементарными ячейками, потому что ребро ячейки все длины одинаковые, а углы ячеек равны 90.
Простая кубическая элементарная ячейка является простейшей повторяющейся
единица в простой кубической структуре. Каждый угол элементарной ячейки
определяется точкой решетки, в которой атом, ион или молекула могут
можно найти в кристалле. По соглашению край элементарной ячейки
всегда соединяет эквивалентные точки. Каждый из восьми углов
поэтому элементарная ячейка должна содержать идентичную частицу. Другой
частицы могут находиться на ребрах или гранях элементарной ячейки,
или в теле элементарной ячейки. Но минимум, который должен быть
для того, чтобы классифицировать элементарную ячейку как простую кубическую,
восемь эквивалентных частиц на восьми углах.
Элементарная объемно-центрированная кубическая ячейка является простейшей повторяющаяся единица в объемно-центрированной кубической структуре. Снова, восемь одинаковых частиц в восьми углах ячейка. Однако на этот раз есть девятая идентичная частица в центре тела элементарной ячейки.
Элементарная гранецентрированная кубическая ячейка также начинается с одинаковые частицы на восьми углах куба. Но это структура также содержит такие же частицы в центрах шесть граней элементарной ячейки, всего 14 одинаковых решеток точки.
Элементарная гранецентрированная кубическая ячейка является простейшей повторяющейся единица в кубической плотноупакованной структуре. На самом деле наличие элементарных гранецентрированных кубических ячеек в этой структуре объясняет, почему структура известна как кубических плотно упакованных.
| Изучение гранецентрированной кубической структуры Деятельность |
Элементарные ячейки: A Трехмерный граф
Точки решетки в элементарной кубической ячейке можно описать в
точки трехмерного графа. Потому что все три ребра ячейки
длины одинаковы в кубической элементарной ячейке, неважно, что
ориентация используется для a , b и c оси. Ради аргумента мы определим ось a как
вертикальной оси нашей системы координат, как показано на
рисунок ниже.
Потому что все три ребра ячейки
длины одинаковы в кубической элементарной ячейке, неважно, что
ориентация используется для a , b и c оси. Ради аргумента мы определим ось a как
вертикальной оси нашей системы координат, как показано на
рисунок ниже.
Ось b затем будет описывать движение поперек фронта элементарной ячейки, а ось c будет представлять движение к задней части элементарной ячейки. Кроме того, мы произвольно определить левый нижний угол элементарной ячейки как начало координат (0,0,0). Координаты 1,0,0 указывают точку решетки, которая одна длина ребра ячейки от начала координат вдоль a ось. Точно так же 0,1,0 и 0,0,1 представляют собой точки решетки, которые смещаются на одну длину ребра клетки от начала координат вдоль б и c осей соответственно.
Рассматривая элементарную ячейку как трехмерный граф
позволяет описать структуру кристалла с
удивительно мало информации. Мы можем указать
структура хлорида цезия, например, всего из четырех частей
информации.
Мы можем указать
структура хлорида цезия, например, всего из четырех частей
информации.
- CsCl кристаллизуется в кубической элементарной ячейке.
- Длина ребра элементарной ячейки 0,4123 нм.
- Имеется Cl — ион в координатах 0,0,0.
- В координатах 1/2,1/2,1/2.
Поскольку край ячейки должен соединять эквивалентные точки решетки, наличие иона Cl — в одном углу блока ячейка (0,0,0) подразумевает наличие иона Cl — при каждый уголок клетки. Координаты 1/2,1/2,1/2 описывают точка решетки в центре клетки. Потому что нет другая точка в элементарной ячейке, которая находится на расстоянии одной длины ребра ячейки по этим координатам это единственный Cs + ион в клетка. Следовательно, CsCl представляет собой простую кубическую элементарную ячейку Cl –. ионы с Cs + в центре тела клетки.
Элементарные ячейки: NaCl и ZnS
NaCl должен кристаллизоваться в плотноупакованный кубический массив Cl — ионы с ионами Na + в октаэдрических отверстиях между
самолеты Cl — ионов. Мы можем перевести эту информацию
в модель элементарной ячейки для NaCl, помня, что
гранецентрированная кубическая элементарная ячейка является простейшей повторяющейся единицей в
кубическая плотнейшая упаковка.
Мы можем перевести эту информацию
в модель элементарной ячейки для NaCl, помня, что
гранецентрированная кубическая элементарная ячейка является простейшей повторяющейся единицей в
кубическая плотнейшая упаковка.
В гранецентрированном кубическом блоке есть четыре уникальных положения. клетка. Эти позиции определяются координатами: 0,0,0; 0,1/2,1/2; 1/2,0,1/2; и 1/2,1/2,0. Наличие частицы в одном углу элементарной ячейки (0,0,0) требует наличия эквивалентная частица на каждом из восьми углов единицы клетка. Поскольку ребро элементарной ячейки соединяет эквивалентные точки, наличие частицы в центре нижней грани (0,1/2,1/2) подразумевает наличие эквивалентной частицы в центр верхней грани (1,1/2,1/2). Точно так же наличие частицы в центре граней 1/2,0,1/2 и 1/2,1/2,0 элементарная ячейка подразумевает эквивалентные частицы в центрах 1/2,1,1/2 и 1/2,1/2,1 грани.
На рисунке ниже показано восьмигранное отверстие в
центр гранецентрированной кубической элементарной ячейки в координатах
1/2,1/2,1/2.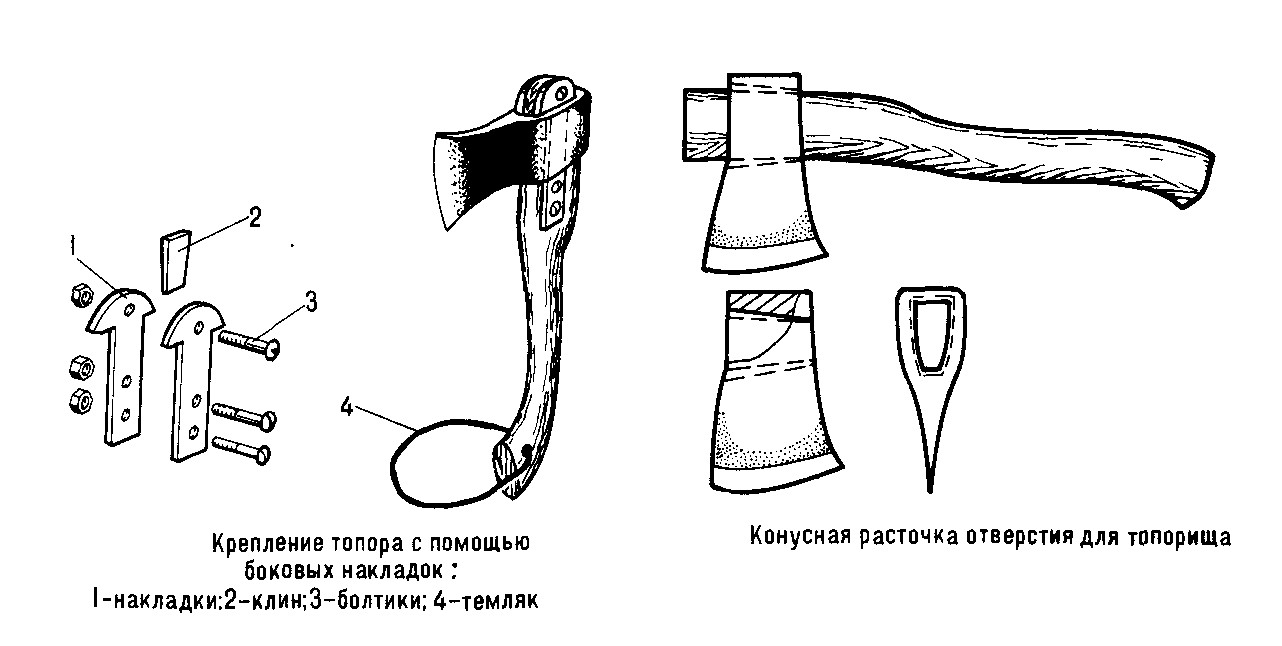 Любая частица в этой точке касается частиц в
центры шести граней элементарной ячейки.
Любая частица в этой точке касается частиц в
центры шести граней элементарной ячейки.
Другие октаэдрические отверстия в гранецентрированной кубической элементарной ячейке находятся по краям ячейки, как показано на рисунке ниже.
Если ионы Cl — занимают узлы решетки элементарная гранецентрированная кубическая ячейка и все октаэдрические отверстия наполнен Na + ионов, мы получаем элементарную ячейку, показанную на рис. рисунок ниже.
Таким образом, мы можем описать структуру NaCl в терминах Следующая информация.
- NaCl кристаллизуется в кубической элементарной ячейке.
- Длина края клетки составляет 0,5641 нм.
- Имеются ионы Cl — в позициях 0,0,0; 1/2,1/2,0; 1/2,0,1/2; и 0,1/2,1/2.
- Имеются ионы Na + в позициях
1/2,1/2,1/2; 1/2,0,0; 0,1/2,0; и 0,0,1/2.

Размещение иона Cl — в этих четырех позициях подразумевает наличие иона Cl — на каждой из 14 решеток точки, определяющие гранецентрированную кубическую единицу. Размещение Na + ион в центре элементарной ячейки (1/2,1/2,1/2) и на трех уникальные ребра элементарной ячейки (1/2,0,0; 0,1/2,0; и 0,0,1/2) требует эквивалентного иона Na + в каждом октаэдре отверстие в элементарной ячейке.
ZnS кристаллизуется в виде кубического плотноупакованного массива S 2- ионы с ионами Zn 2+ в тетраэдрических дырках. S 2- ионы в этом кристалле занимают те же позиции, что и Cl — ионы в NaCl. Единственная разница между этими кристаллами заключается в
расположение положительных ионов. На рисунке ниже показано, что
тетраэдрические отверстия в гранецентрированной кубической элементарной ячейке находятся в
углы элементарной ячейки в координатах 1/4,1/4,1/4. Ан
атом с этими координатами коснулся бы атома в этом углу
а также атомы в центрах трех граней, образующих
этот угол.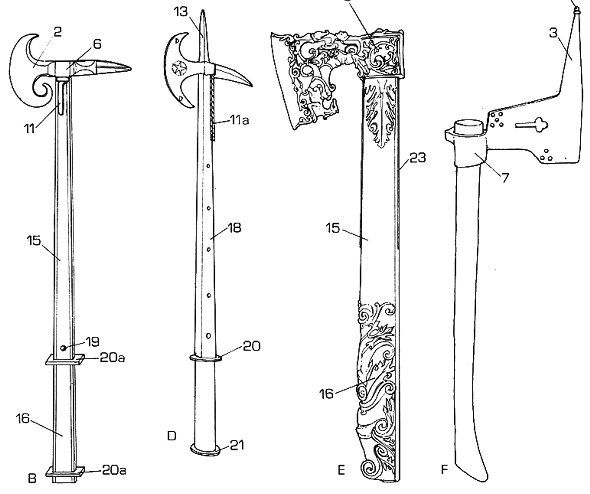 Хотя это трудно увидеть без
трехмерная модель, четыре атома, окружающие это отверстие
расположены по углам тетраэдра.
Хотя это трудно увидеть без
трехмерная модель, четыре атома, окружающие это отверстие
расположены по углам тетраэдра.
Поскольку углы элементарной кубической ячейки одинаковы, должно быть четырехгранное отверстие в каждом из восьми углов элементарная гранецентрированная кубическая ячейка. Если ионы S 2- занимают точки решетки гранецентрированной кубической элементарной ячейки и Zn 2+ ионы упакованы в каждую вторую тетраэдрическую дырку, мы получаем элементарная ячейка ZnS показана на рисунке ниже.
Таким образом, структуру ZnS можно описать следующим образом.
- ZnS кристаллизуется в кубической элементарной ячейке.
- Длина края клетки составляет 0,5411 нм.
- Имеются ионы S 2- в позициях 0,0,0; 1/2,1/2,0; 1/2,0,1/2; и 0,1/2,1/2.
- Имеются ионы Zn 2+ в позициях
1/4,1/4,1/4; 1/4,3/4,3/4; 3/4,1/4,3/4; и 3/4,3/4,1/4.

Обратите внимание, что в этот кристалл, потому что на каждое S 9 приходится два тетраэдрических отверстия.0215 2- ион в наиболее плотно упакованном массиве этих ионов.
Элементарные ячейки: измерение Расстояние между частицами
Никель — один из металлов, кристаллизующихся в кубической форме. плотно упакованная структура. Если учесть, что атом никеля имеет массу всего 9,75 х 10 -23 г и ионный радиус всего 1,24 x 10 90 215 -10 90 216 м, это замечательное достижение уметь описать структуру этого металла. Очевидное вопрос: откуда мы знаем, что никель упаковывается в кубический наиболее плотно упакованная структура?
Единственный способ определить структуру вещества на атомном Масштаб заключается в использовании зонда еще меньшего размера. Один из многих полезные зонды для изучения материи в таком масштабе электромагнитное излучение.
В 1912 году Макс ван Лауэ обнаружил, что рентгеновские лучи, попавшие в
поверхности кристалла дифрагировали в узоры, напоминающие
узоры, возникающие при прохождении света через очень узкую
щель. Вскоре после этого Уильям Лоуренс Брэгг, который только что
получил степень бакалавра физики в Кембридже,
объяснил результаты ван Лауэ с помощью уравнения, известного как Брэгг
уравнение , которое позволяет нам рассчитать расстояние между
плоскостях атомов в кристалле по картине дифракции
рентгеновские лучи известной длины волны.
Вскоре после этого Уильям Лоуренс Брэгг, который только что
получил степень бакалавра физики в Кембридже,
объяснил результаты ван Лауэ с помощью уравнения, известного как Брэгг
уравнение , которое позволяет нам рассчитать расстояние между
плоскостях атомов в кристалле по картине дифракции
рентгеновские лучи известной длины волны.
п = 2 d sin T
Схема, по которой рентгеновские лучи дифрагируют на металлическом никеле предполагает, что этот металл упаковывается в элементарную кубическую ячейку с расстояние между плоскостями атомов 0,3524 нм. Таким образом длина ребра ячейки в этом кристалле должна быть 0,3524 нм. Знаю это никель кристаллизуется в кубической элементарной ячейке недостаточно. Мы все еще должны решить, является ли это простой кубической, объемно-центрированной кубической, или гранецентрированная кубическая элементарная ячейка. Это можно сделать, измерив плотность металла.
Единичные ячейки: определение Элементарная ячейка кристалла
Атомы на углах, ребрах и гранях элементарной ячейки
разделены более чем одной элементарной ячейкой, как показано на рисунке ниже. Атом на грани разделен двумя элементарными ячейками, поэтому только половина
атом принадлежит каждой из этих ячеек. Атом на краю
разделены четырьмя элементарными ячейками, а атом на углу разделен
восемь элементарных ячеек. Таким образом, только четверть атома на ребре
и одна восьмая часть атома на углу может быть отнесена к каждому из
элементарные ячейки, которые разделяют эти атомы.
Атом на грани разделен двумя элементарными ячейками, поэтому только половина
атом принадлежит каждой из этих ячеек. Атом на краю
разделены четырьмя элементарными ячейками, а атом на углу разделен
восемь элементарных ячеек. Таким образом, только четверть атома на ребре
и одна восьмая часть атома на углу может быть отнесена к каждому из
элементарные ячейки, которые разделяют эти атомы.
Если никель кристаллизовался в простой кубической элементарной ячейке, то будет атом никеля на каждом из восьми углов ячейки. Поскольку только одна восьмая часть этих атомов может быть отнесена к данному элементарная ячейка, каждая элементарная ячейка в простой кубической структуре будет иметь один чистый атом никеля.
Простая кубическая структура:
8 углов x 1/8 = 1 атом
Если бы никель образовывал объемно-центрированную кубическую структуру,
быть два атома на элементарную ячейку, потому что атом никеля в центре
тела не будет делиться ни с какими другими элементарными ячейками.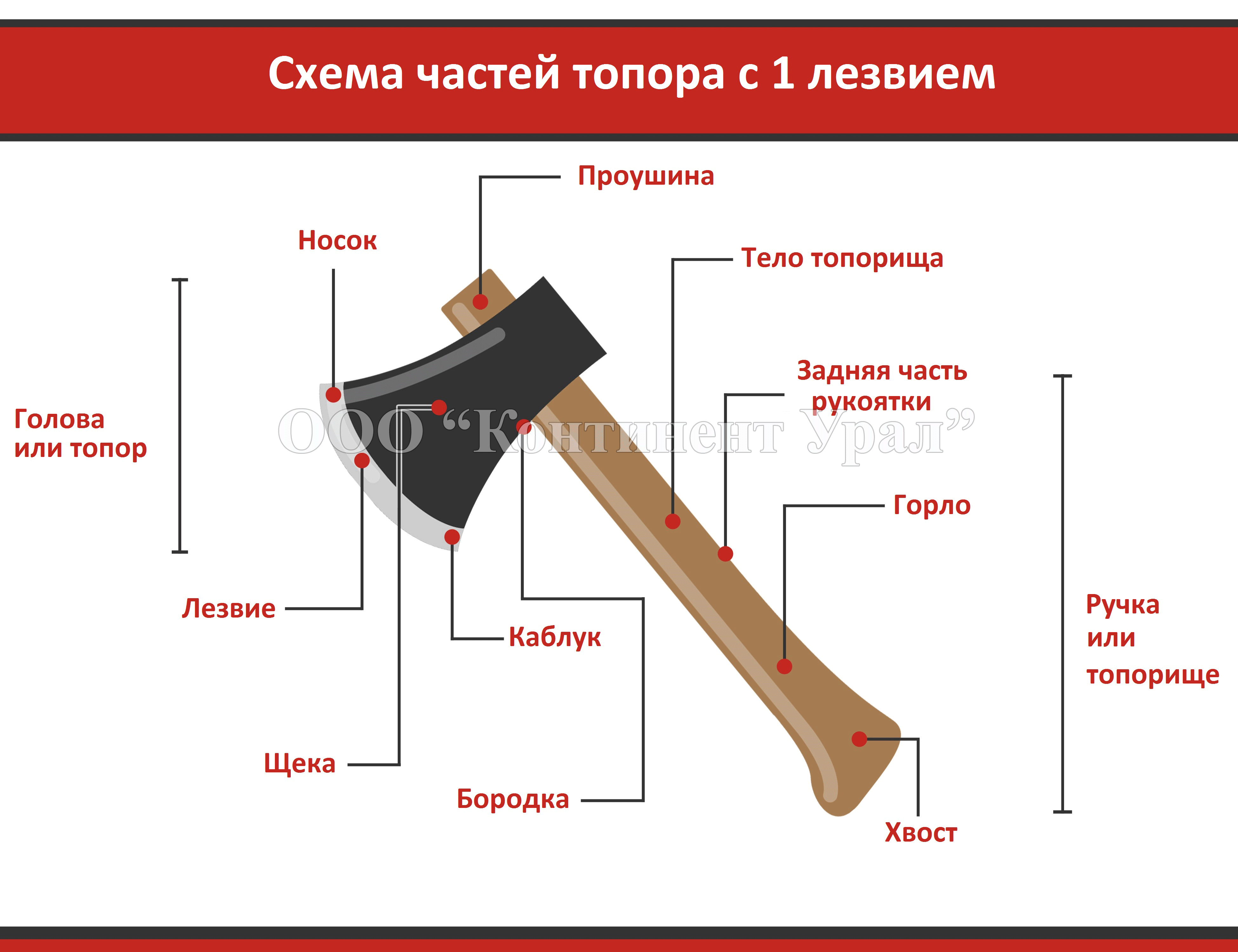
Объемно-центрированная кубическая структура:
(8 углов x 1/8) + 1 тело = 2 атома
Если никель кристаллизуется в гранецентрированной кубической структуре, шесть атомов на гранях элементарной ячейки внесли бы три чистые атомы никеля, всего четыре атома на элементарную ячейку.
Гранецентрированная кубическая структура:
(8 углов x 1/8) + (6 граней x 1/2) = 4 атома
Поскольку они имеют разное количество атомов в элементарной ячейке, каждая из этих структур будет иметь разную плотность. Давайте поэтому рассчитывайте плотность никеля на основе каждого из этих структуры и длина ребра элементарной ячейки для никеля, приведенные в предыдущий участок: 0,3524 нм. Для этого нам нужно знать объем элементарной ячейки в кубических сантиметрах и масса один атом никеля.
Объем ( V ) элементарной ячейки равен длина ребра ячейки ( a ) в кубе.
В = a 3 = (0,3524 нм) 3 = 0,04376 нм 3
Так как в метре 10 9 нм и 10 0 см в
метр, в см должно быть 10 7 нм.
Следовательно, мы можем перевести объем элементарной ячейки в см 3 следующее.
Массу атома никеля можно рассчитать по атомному вес этого металла и число Авогадро.
Плотность никеля, если он кристаллизовался в простой кубической структуры, следовательно, будет 2,23 г/см 3 , до трех значимые фигуры.
Простая кубическая структура:
Потому что в элементарной ячейке было бы вдвое больше атомов, если бы никель кристаллизуется в объемно-центрированную кубическую структуру, плотность никеля в этой структуре была бы вдвое больше.
Объемно-центрированная кубическая структура:
На элементарную ячейку в гранецентрированной кубическая структура и плотность никеля в этой структуре будет быть в четыре раза больше.
Гранецентрированная кубическая структура:
Экспериментальное значение плотности никеля составляет 8,90 г/см 3 .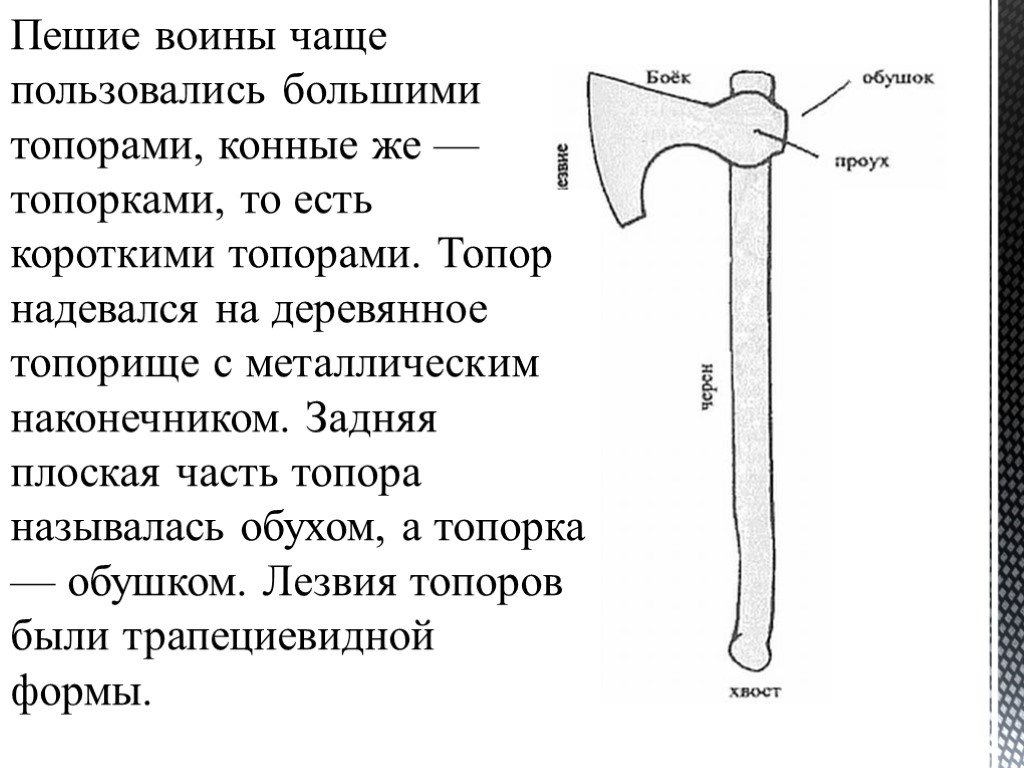 Очевидный вывод состоит в том, что никель кристаллизуется в
гранецентрированная кубическая элементарная ячейка и, следовательно, имеет кубическую
плотно упакованная структура.
Очевидный вывод состоит в том, что никель кристаллизуется в
гранецентрированная кубическая элементарная ячейка и, следовательно, имеет кубическую
плотно упакованная структура.
Единичные ячейки: расчет Металлические или ионные радиусы
Можно найти оценки радиусов большинства атомов металлов. Где откуда эти данные? Откуда мы знаем, например, что радиус атома никеля равен 0,1246 нм?
Никель кристаллизуется в элементарной гранецентрированной кубической ячейке с длина ребра ячейки 0,3524 нм для расчета радиуса никеля атом.
Показана одна из граней гранецентрированной кубической элементарной ячейки на рисунке ниже.
Согласно этому рисунку, диагональ на лицевой стороне этого Элементарная ячейка в четыре раза больше радиуса атома никеля.
Теорема Пифагора утверждает, что диагональ
прямоугольный треугольник равен сумме квадратов другого
стороны. Таким образом, диагональ, проходящая через грань элементарной ячейки, равна
связано с длиной ребра элементарной ячейки следующим уравнением.
Таким образом, диагональ, проходящая через грань элементарной ячейки, равна
связано с длиной ребра элементарной ячейки следующим уравнением.
Извлечение квадратного корня из обеих сторон дает следующее результат.
Теперь подставим в это уравнение соотношение между диагональ через грань этой элементарной ячейки и радиус атом никеля:
Решение для радиуса атома никеля дает значение 0,1246 нм:
Аналогичный подход можно использовать для оценки размера ион. Начнем с того, что длина ребра ячейки в хлорида цезия составляет 0,4123 нм, чтобы рассчитать расстояние между центры Cs + и Cl — ионов в CsCl.
CsCl кристаллизуется в простой кубической элементарной ячейке Cl — ионы с ионом Cs + в центре тела ячейки, как показано на рисунке ниже.
Прежде чем мы сможем вычислить расстояние между центрами
ионы Cs + и Cl — в этом кристалле,
однако мы должны признать правомерность одного из простейших
предположения об ионных твердых телах: положительные и отрицательные ионы
которые образуют эти кристаллы касания.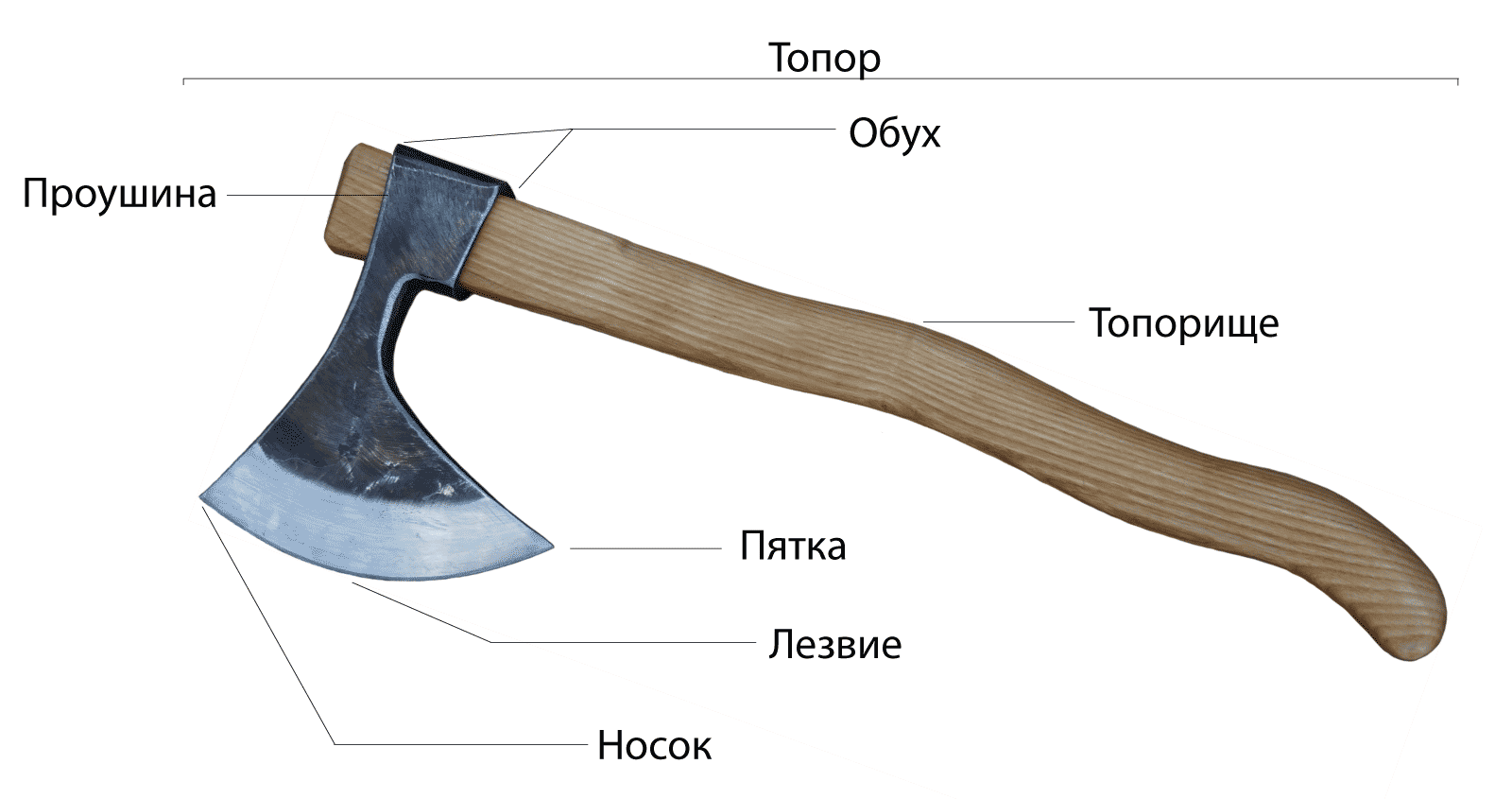
Таким образом, мы можем предположить, что диагональ тела элементарная ячейка CsCl эквивалентна сумме радиусов двух Ионы Cl — и два иона Cs + .
Трехмерный эквивалент теоремы Пифагора предполагает, что квадрат диагонали через тело куб это сумма квадратов трех сторон.
Извлечение квадратного корня из обеих частей этого уравнения дает следующий результат.
Если длина ребра клетки в CsCl равна 0,4123 нм, диагональ поперек тела в этой элементарной ячейке составляет 0,7141 нм.
Сумма ионных радиусов Cs + и Cl — ионов составляет половину этого расстояния, или 0,3571 нм.
Если бы у нас была оценка размера Cs + или ион Cl — , мы могли бы использовать результаты для расчета
радиус другого иона. Ионный радиус Cl — ион составляет 0,181 нм.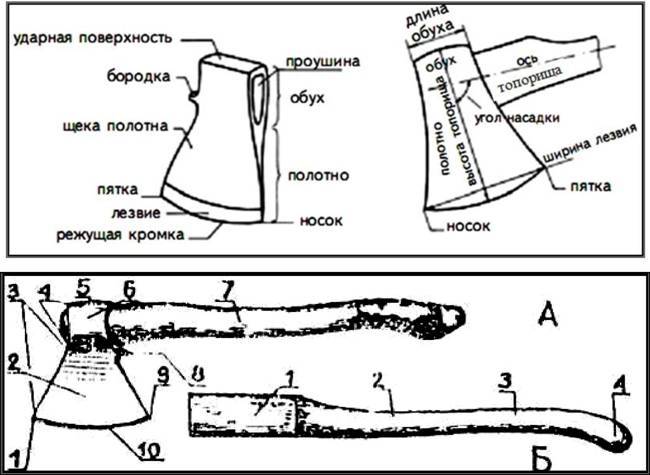

 Полярность
этих связей уравновешивается, делая молекулу неполярной.
Полярность
этих связей уравновешивается, делая молекулу неполярной.
 молекула должна быть полярной.
молекула должна быть полярной. В экваториальных положениях, начиная с одного положения
занимает одинокая пара, они не компенсируются, и
молекула полярна.
В экваториальных положениях, начиная с одного положения
занимает одинокая пара, они не компенсируются, и
молекула полярна.